К 20-м годам XX века физики уже не сомневались в том, что атомные ядра, открытые Э. Резерфордом в 1911 г., также как и сами атомы, имеют сложную структуру. В этом их убеждали многочисленные экспериментальные факты, накопленные к этому времени: открытие радиоактивности, экспериментальное доказательство ядерной модели атома, измерение отношения e / m для электрона, α-частицы и для так называемой H-частицы – ядра атома водорода, открытие искусственной радиоактивности и ядерных реакций, измерение зарядов атомных ядер и т. д.
В настоящее время твердо установлено, что атомные ядра различных элементов состоят из частиц двух видов – протонов и нейтронов.
Первая из этих частиц представляет собой атом водорода, из которого удален единственный электрон. Эта частица наблюдалась уже в 1907 г. в опытах Дж. Томсона, которому удалось измерить у нее отношение e / m. В 1919 году Э. Резерфорд обнаружил ядра атома водорода в продуктах расщепления ядер атомов многих элементов. Резерфорд назвал эту частицу протоном. Он высказал предположение, что протоны входят в состав всех атомных ядер. Схема опытов Резерфорда представлена на рис. 6.5.1.
|
|
|
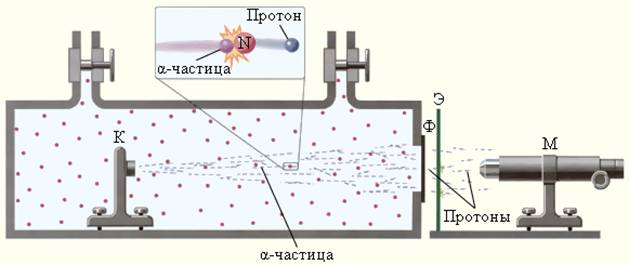
Рисунок 6.5.1. Схема опытов Резерфорда по обнаружению протонов в продуктах расщепления ядер. К – свинцовый контейнер с радиоактивным источником α-частиц, Ф – металлическая фольга, Э – экран, покрытый сульфидом цинка, М – микроскоп |
Прибор Резерфорда состоял из вакуумированной камеры, в которой был расположен контейнер К с источником α-частиц. Окно камеры было закрыто металлической фольгой Ф, толщина которой была подобрана так, чтобы α-частицы не могли через нее проникнуть. За окном располагался экран Э, покрытый сернистым цинком. С помощью микроскопа М можно было наблюдать сцинтилляции (т. е. световые вспышки) в точках попадания на экран тяжелых заряженных частиц. При заполнении камеры азотом низкого давления на экране возникали световые вспышки, указывающие на появление потока каких-то частиц, способных проникать через фольгу Ф, практически полностью задерживающую поток α-частиц. Отодвигая экран Э от окна камеры, Резерфорд измерил среднюю длину свободного пробега наблюдаемых частиц в воздухе. Она оказалась приблизительно равной 28 см, что совпадало с оценкой длины пробега H-частиц, наблюдавшихся ранее Дж. Томсоном. Исследования действия на частицы, выбиваемые из ядер азота, электрических и магнитных полей показали, что эти частицы обладают положительным элементарным зарядом и их масса равна массе ядра атома водорода. Впоследствии опыт был выполнен с целым рядом других газообразных веществ. Во всех случаях было обнаружено, что из ядер этих веществ α-частицы выбивают H-частицы или протоны.
По современным измерениям, положительный заряд протона в точности равен элементарному заряду e = 1,60217733·10–19 Кл, то есть равен по модулю отрицательному заряду электрона. В настоящее время равенство зарядов протона и электрона проверено с точностью 10–22. Такое совпадение зарядов двух непохожих друг на друга частиц вызывает удивление и остается одной из фундаментальных загадок современной физики.
Масса протона, по современным измерениям, равна mp = 1,67262∙10–27 кг. В ядерной физике массу частицы часто выражают в атомных единицах массы (а. е. м.), равной ![]() массы атома углерода с массовым числом 12:
массы атома углерода с массовым числом 12:
|
1 а. е. м. = 1,66057·10–27 кг. |
Следовательно, mp = 1,007276 а. е. м. Во многих случаях массу частицы удобно выражать в эквивалентных значениях энергии в соответствии с формулой E = mc2. Так как 1 эВ = 1,60218·10–19 Дж, в энергетических единицах масса протона равна 938,272331 МэВ.
Таким образом, в опыте Резерфорда было открыто явление расщепления ядер азота и других элементов при ударах быстрых α-частиц и показано, что протоны входят в состав ядер атомов.
После открытия протона было высказано предположение, что ядра атомов состоят из одних протонов. Однако это предположение оказалось несостоятельным, так как отношение заряда ядра к его массе не остается постоянным для разных ядер, как это было бы, если бы в состав ядер входили одни протоны. Для более тяжелых ядер это отношение оказывается меньше, чем для легких, т. е. при переходе к более тяжелым ядрам масса ядра растет быстрее, чем заряд.
В 1920 г. Резерфорд высказал гипотезу о существовании в составе ядер жестко связанной компактной протон-электронной пары, представляющей собой электрически нейтральное образование – частицу с массой, приблизительно равной массе протона. Он даже придумал название этой гипотетической частице – нейтрон. Это была очень красивая, но, как выяснилось впоследствии, ошибочная идея. Электрон не может входить в состав ядра. Квантово-механический расчет на основании соотношения неопределенностей показывает, что электрон, локализованный в ядре, т. е. области размером R ≈ 10–13 см, должен обладать колоссальной кинетической энергией, на много порядков превосходящей энергию связи ядер в расчете на одну частицу. Однако идея о существовании тяжелой нейтральной частицы казалась Резерфорду настолько привлекательной, что он незамедлительно предложил группе своих учеников во главе с Джеймсом Чедвиком заняться ее поиском. Через 12 лет, в 1932 г. Чедвик экспериментально исследовал излучение, возникающее при облучении бериллия α-частицами, и обнаружил, что это излучение представляет собой поток нейтральных частиц с массой, примерно равной массе протона. Так был открыт нейтрон. На рис. 6.5.2 приведена упрощенная схема установки для обнаружения нейтронов.
|
|
|
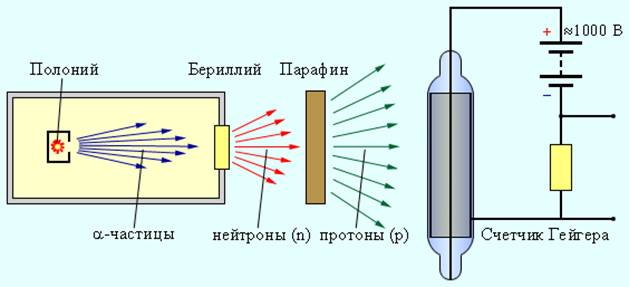
Рисунок 6.5.2. Схема установки для обнаружения нейтронов |
При бомбардировке бериллия α-частицами, испускаемыми радиоактивным полонием, возникает сильное проникающее излучение, способное преодолеть такую преграду, как слой свинца толщиной в 10–20 см. Это излучение почти одновременно с Чедвиком наблюдали супруги Ирен и Фредерик Жолио-Кюри (Ирен – дочь Марии и Пьера Кюри), но они предположили, что это γ-лучи большой энергии. Они обнаружили, что если на пути излучения бериллия поставить парафиновую пластину, то ионизирующая способность этого излучения резко возрастает. Они доказали, что излучение бериллия выбивает из парафина протоны, которые в большом количестве имеются в этом водородосодержащем веществе. По длине свободного пробега протонов в воздухе они оценили энергию γ-квантов, способных при столкновении сообщить протонам необходимую скорость. Она оказалась огромной – порядка 50 МэВ.
Дж. Чедвик в 1932 г. выполнил серию экспериментов по всестороннему изучению свойств излучения, возникающего при облучении бериллия α-частицами. В своих опытах Чедвик использовал различные методы исследования ионизирующих излучений. На рис. 6.5.2 изображен счетчик Гейгера, предназначенный для регистрации заряженных частиц. Он состоит из стеклянной трубки, покрытой изнутри металлическим слоем (катод), и тонкой нити, идущей вдоль оси трубки (анод). Трубка заполняется инертным газом (обычно аргоном) при низком давлении. Заряженная частица, пролетая в газе, вызывает ионизацию молекул. Появившиеся в результате ионизации свободные электроны ускоряются электрическим полем между анодом и катодом до энергий, при которых начинается ударная ионизация. Возникает лавина ионов, и через счетчик проходит короткий разрядный импульс тока. Другим важнейшим прибором для исследования частиц является так называемая камера Вильсона, в которой быстрая заряженная частица оставляет след (трек). Траекторию частицы можно наблюдать непосредственно или фотографировать. Действие камеры Вильсона, созданной в 1912 г., основано на конденсации перенасыщенного пара на ионах, образующихся в рабочем объеме камеры вдоль траектории заряженной частицы. С помощью камеры Вильсона можно наблюдать искривление траектории заряженной частицы в электрическом и магнитном полях.
Дж. Чедвик в своих опытах наблюдал в камере Вильсона треки ядер азота, испытавших столкновение с бериллиевым излучением. На основании этих опытов он сделал оценку энергии γ-кванта, способного сообщить ядрам азота наблюдаемую в эксперименте скорость. Она оказалась равной 100–150 МэВ. Такой огромной энергией не могли обладать γ-кванты, испущенные бериллием. На этом основании Чедвик заключил, что из бериллия под действием α-частиц вылетают не безмассовые γ-кванты, а достаточно тяжелые частицы. Эти частицы обладали большой проникающей способностью и непосредственно не ионизировали газ в счетчике Гейгера, следовательно, они были электронейтральны. Так было доказано существование нейтрона – частицы, предсказанной Резерфордом более чем за 10 лет до опытов Чедвика.
Нейтрон – это элементарная частица. Ее не следует представлять в виде компактной протон-электронной пары, как первоначально предполагал Резерфорд.
По современным измерениям, масса нейтрона mn = 1,67493∙10–27 кг = 1,008665 а. е. м. В энергетических единицах масса нейтрона равна 939,56563 МэВ. Масса нейтрона приблизительно на две электронные массы превосходит массу протона.
Сразу же после открытия нейтрона российский ученый Д.Д Иваненко и немецкий физик В. Гейзенберг выдвинули гипотезу о протонно-нейтронном строении атомных ядер, которая полностью подтвердилась последующими исследованиями. Протоны и нейтроны принято называть нуклонами.
Для характеристики атомных ядер вводится ряд обозначений. Число протонов, входящих в состав атомного ядра, обозначают символом Z и называют зарядовым числом или атомным номером (это порядковый номер в периодической таблице Менделеева). Заряд ядра равен Ze, где e – элементарный заряд. Число нейтронов обозначают символом N.
Общее число нуклонов (т. е. протонов и нейтронов) называют массовым числом A:
|
A = Z + N. |
Ядра химических элементов обозначают символом ![]() , где X – химический символ элемента. Например,
, где X – химический символ элемента. Например,
![]() – водород,
– водород, ![]() – гелий,
– гелий, ![]() – углерод,
– углерод, ![]() – кислород,
– кислород, ![]() – уран.
– уран.
Ядра одного и того же химического элемента могут отличаться числом нейтронов. Такие ядра называются изотопами. У большинства химических элементов имеется несколько изотопов. Например, у водорода их три: ![]() – обычный водород,
– обычный водород, ![]() – дейтерий и
– дейтерий и ![]() – тритий. У углерода – 6 изотопов, у кислорода – 3.
– тритий. У углерода – 6 изотопов, у кислорода – 3.
Химические элементы в природных условиях обычно представляют собой смесь изотопов. Существование изотопов определяет значение атомной массы природного элемента в периодической системе Менделеева. Так, например, относительная атомная масса природного углерода равна 12,011.